近期一支国际联合科研团队在顶级期刊《自然·通讯》上发表了一项具有里程碑意义的研究。他们首次成功开发出一种靶向新型大脑受体“代谢型甘氨酸受体(mGlyR)”的纳米抗体(Nb20),并通过非侵入性的鼻内给药方式,在小鼠模型中实现了快速、强效且持久的抗抑郁效果。这项研究不仅验证了mGlyR作为抗抑郁新靶点的巨大潜力,更展示了纳米抗体作为治疗脑部疾病新型生物制剂的可行性,为难以治愈的神经精神疾病带来了全新的治疗范式。
那么,这项被誉为“里程碑”的研究具体取得了哪些关键发现?其作用机制又是怎样的?
研究背景:抑郁症治疗的困境与新靶点的发现
重度抑郁症(MDD)全球高发,现有主流药物多靶向单胺能系统(如5-羟色胺、去甲肾上腺素),存在起效慢(数周)、有效率有限、副作用多等问题,急需新机制疗法。2019年,本研究的作者之一Kirill A. Martemyanov发现并命名了mGlyR(由孤儿受体GPR158转化而来)。该受体在大脑前额叶皮层(PFC)高表达,在应激和抑郁症患者中显著上调。遗传学研究表明,敲除mGlyR可使小鼠产生抗抑郁表态和应激韧性,使其成为极富吸引力的药物新靶点。mGlyR的机制与传统GPCR不同,mGlyR不直接偶联G蛋白,而是通过调控RGS7/Gβ5复合物的GAP(GTP酶活化蛋白)活性来影响下游信号。甘氨酸是其内源性配体,但起的是抑制受体功能的作用。
背景核心技术:为何选择纳米抗体
面对mGlyR这一缺乏高选择性化学探针的膜蛋白靶点,研究团队选择了纳米抗体(单域抗体), 这一新兴工具有以下特点:
高亲和力与高特异性:源于羊驼,仅由一个重链可变域(VHH)构成,体积小但结合力强。
精准靶向:可精准识别特定构象的胞外域,适合干预像mGlyR这样具有大胞外区的受体。
稳定性好,易于生产:可在细菌系统中大量表达,成本相对较低。
潜在的脑部递送优势:小尺寸有助于通过血脑屏障或其它非侵入途径(如鼻-脑通路)递送。
关键发现与数据解读
关成功筛选出高亲和力、高特异性纳米抗体Nb20
开发流程:用mGlyR免疫羊驼,构建噬菌体展示文库,经过多轮高通量筛选,从筛选后的61个克隆中鉴定出结合力最强的克隆——Nb20(见图1a)。
结合特性:流式细胞术显示其与细胞膜上mGlyR结合的EC50约为 10 nM(见图1d,e)。表面等离子共振(SPR)测得与纯化受体胞外域结合的KD为 375 nM(细胞实验亲和力更高可能因多价效应)(见图1f,g)。
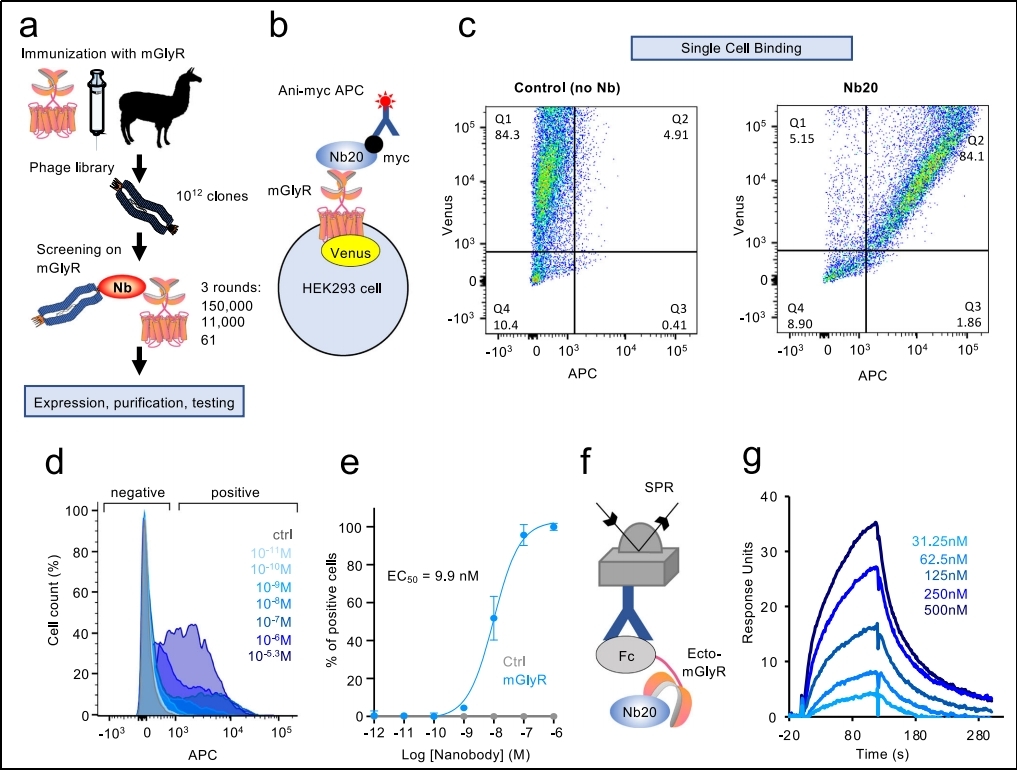 图1 mGlyR纳米抗体的开发和验证
图1 mGlyR纳米抗体的开发和验证
关键验证:Nb20的结合不被甘氨酸影响,且不结合其他相关GPCR,证明了其独特且特异的结合表位。
Nb20特异性抑制mGlyR-RGS7/Gβ5复合物的GAP活性
功能验证: 在基于BRET的GAP活性检测中,Nb20能特异性抑制由mGlyR-RGS7/Gβ5复合物介导的Gαo蛋白失活,IC50约为 6 nM。这表明Nb20模拟了内源性配体甘氨酸的“抑制”作用(见图2b,c,d,e)。
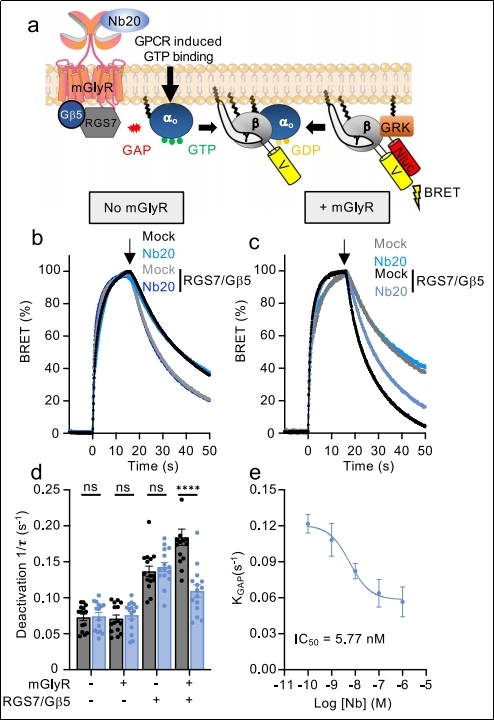 图2 Nb20对mGlyR-RGS7/ Gβ5 复合物GAP活性的调控
图2 Nb20对mGlyR-RGS7/ Gβ5 复合物GAP活性的调控
冷冻电镜揭示作用机制:从胞外到保内的构象重塑
结构解析:研究团队成功解析了Nb20-mGlyR以及Nb20-mGlyR-RGS7/Gβ5复合物的冷冻电镜结构(分辨率分别为3.49Å和3.89Å)(见图3a,b)。
结合位点:Nb20结合在mGlyR二聚体两个Cache结构域(配体结合域)侧面的交界处,主要通过其CDR1和CDR2环与受体相互作用(见图3c,d)。
构象变化:与未结合的受体相比,Nb20的结合导致受体胞外域(ECD)发生了高达12Å的平移和7°的旋转。这种变化通过跨膜区传递至胞内。
作用机制推论:Nb20的结合稳定了受体的某种构象,导致与其相互作用的RGS7/Gβ5复合物(尤其是其催化RGS结构域)变得高度柔性,无法有效定位并催化膜上的Gα蛋白,从而阻断了信号传导。这为“抑制”功能提供了结构基础。
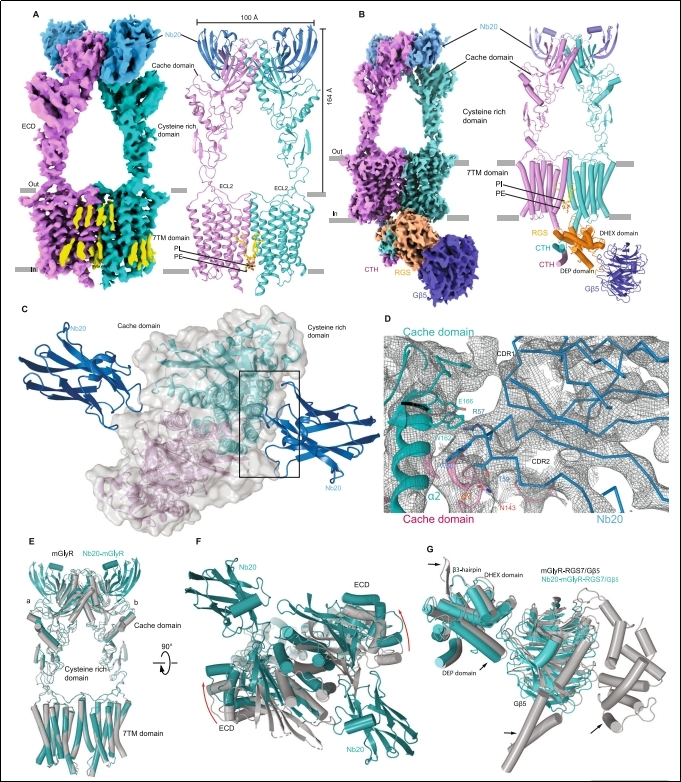 图3 含Nb20的mGlyRin复合物的冷冻电镜结构
图3 含Nb20的mGlyRin复合物的冷冻电镜结构
动物模型验证:卓越的抗抑郁疗效
直接脑内注射:侧脑室注射Nb20后,小鼠在埋珠实验、悬尾实验、强迫游泳实验中均表现出显著的抗抑郁样行为,效果可持续至少两周(见图4a,b,c)。
疗效非侵入性鼻内给药(核心亮点):在慢性可变应激诱导的抑郁症小鼠模型中,鼻内给予Nb20产生了与快速抗抑郁药氯胺酮(Ketamine)疗效相当的强劲效果,且在两性中均有效。
特异性与安全性验证:结合能力缺失的突变体Nb20无任何效果,证明了作用靶点特异性(见图4d,e)。Nb20不影响小鼠的自主活动、运动协调能力及快感行为。
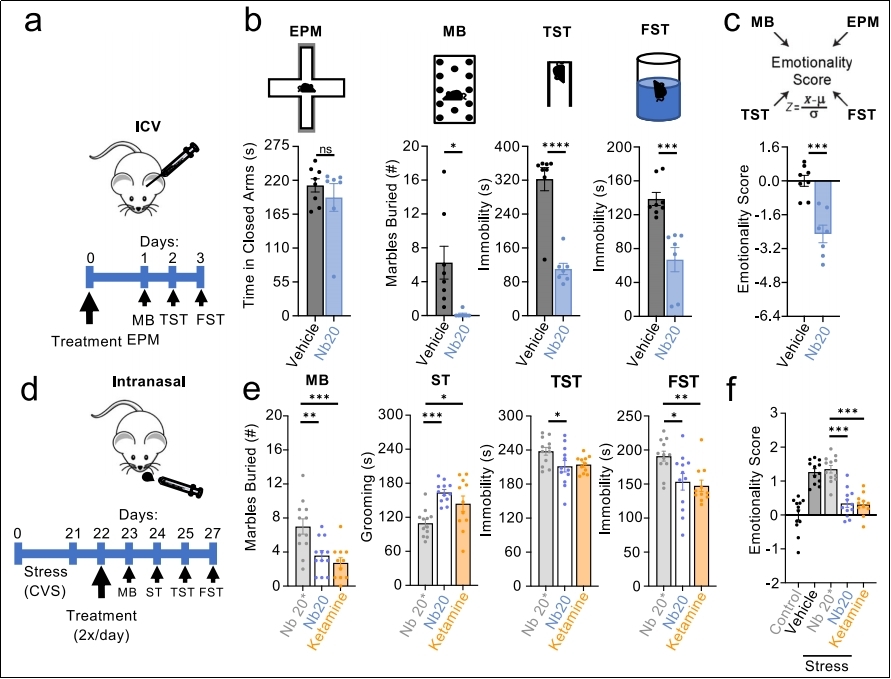 图4 Nb20给药对小鼠抗抑郁效果的影响
图4 Nb20给药对小鼠抗抑郁效果的影响
对神经环路的影响:增加前额叶皮层神经元兴奋性
在脑片电生理实验中,Nb20处理可显著增加前边缘皮层II-III层锥体神经元的兴奋性(动作电位发放增多,阈值电流降低),这与敲除mGlyR或使用甘氨酸抑制的效果一致,从环路水平解释了其可能起效的原因(见图5)。
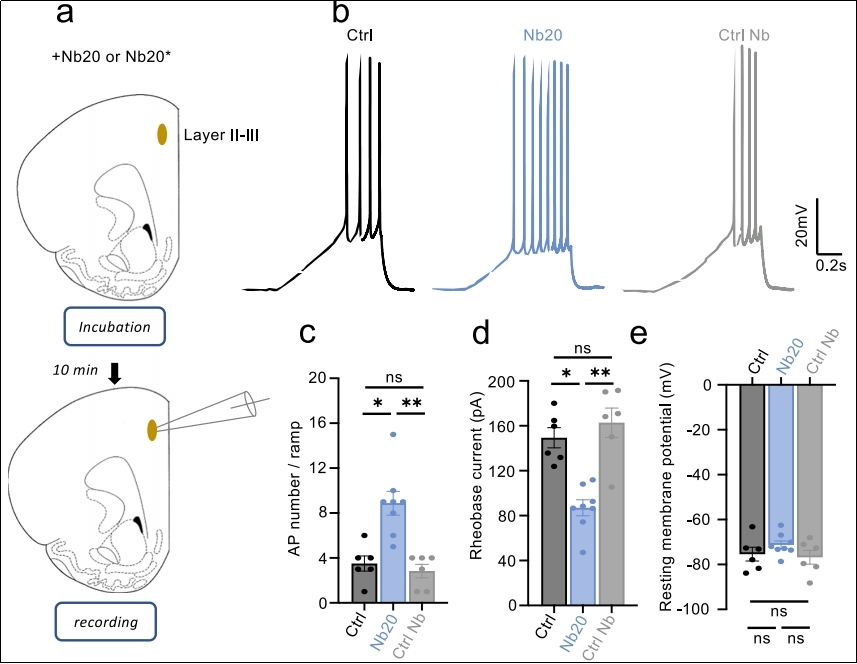 图5 Nb20对神经元兴奋性的影响
图5 Nb20对神经元兴奋性的影响
研究结论和意义
结论:这项研究是神经科学、结构生物学与抗体工程学交叉融合的典范。它不仅仅发现了一个有效的抗抑郁纳米抗体,更打开了一扇大门:证明了利用高特异性、可非侵入性递送的纳米抗体来精准调控大脑中难以成药的GPCR靶点,进而治疗重大神经精神疾病,是一条充满希望的崭新路径。这为无数饱受抑郁困扰的患者带来了新的曙光,也为生物医药产业开发下一代神经精神疾病疗法指明了创新方向。
意义:本研究中的治疗模式创新是首次将纳米抗体免疫疗法应用于抑郁症等情绪障碍治疗,突破了传统小分子和生物大分子药物的局限,并且成功演示了鼻内给药这种非侵入方式可将纳米抗体有效递送至大脑并发挥功能,极大地提升了临床转化的便利性和患者依从性,为mGlyR作为下一代抗抑郁药靶点提供了最强有力的工具化合物和概念验证。
此项研究也凸显了强大的抗体发现与工程平台在转化医学中的核心价值。而我们纳博生命拥有NabLib®平台所具备的 pDual改进型双功能噬菌体展示技术,能够在传统噬菌体展示的高效开发的基础上,无缝衔接哺乳动物细胞高效生产,大大提高筛除问题分子的效率;NabLib®哺乳动物细胞展示技术,不仅可以提升筛选分子的可开发性,还可以灵活地选择抗体的筛选构型,为下游抗体分子的应用和检测提供更好的保障。

武汉纳博生命科技有限公司是由武汉产业创新发展研究院牵头成立建设的纳米抗体产业平台。其总部位于武汉东湖新技术开发区武创院本部大楼,在武汉生物城精准医疗产业基地拥有占地面积达1400㎡的自主实验室,并在武汉左岭与黄冈团风分别建立了符合实验动物标准的羊驼实验基地与转运基地,目前基地在饲养的羊驼共600余头,可为科研机构及抗体药物研发企业提供“零免疫背景”保障的羊驼免疫服务。
纳博生命专注于纳米抗体开发、改造与应用,致力于构建产、学、研一体化的实验公共服务平台。现拥有从抗原制备(多肽、蛋白及RNA),到抗体发现和抗体工程,再到生物学功能验证/筛选的全链路技术平台。其中RNA抗原包括针对羊驼进行RNA结构和序列优化的RNA;抗体发现与抗体工程服务采用噬菌体展示、哺乳动物细胞展示在内的多种技术路线。通过多平台的交叉互补为药企及科研院所提供灵活的抗体发现及改造服务,助力药物试剂的研发。
联系方式:400-822-9180
联系邮箱:marketingdept@nanobodylife.com








 图1 mGlyR纳米抗体的开发和验证
图1 mGlyR纳米抗体的开发和验证 图2 Nb20对mGlyR-RGS7/ Gβ5 复合物GAP活性的调控
图2 Nb20对mGlyR-RGS7/ Gβ5 复合物GAP活性的调控 图3 含Nb20的mGlyRin复合物的冷冻电镜结构
图3 含Nb20的mGlyRin复合物的冷冻电镜结构 图4 Nb20给药对小鼠抗抑郁效果的影响
图4 Nb20给药对小鼠抗抑郁效果的影响 图5 Nb20对神经元兴奋性的影响
图5 Nb20对神经元兴奋性的影响