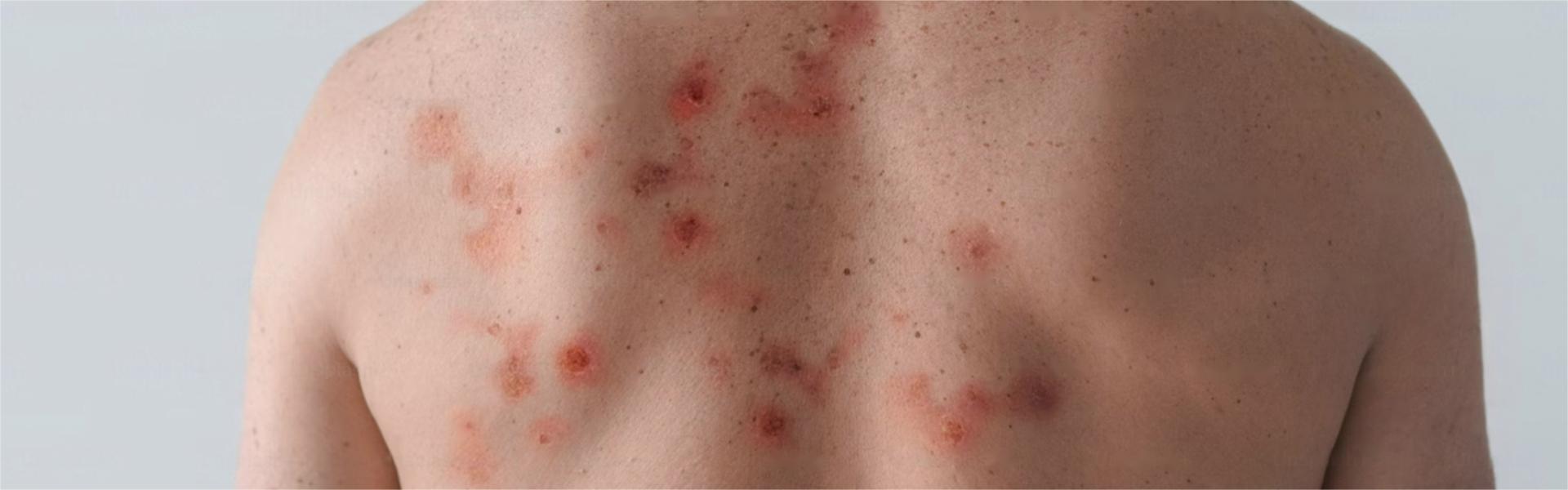
银屑病在所有年龄阶段且无论男女均有发生的可能性,具有家族病史的人比常人更易发生。主要病症为皮肤出现鳞样屑性红斑伴有大量脱皮、瘙痒、疼痛等特征,部分患者可同时出现关节损害的症状,严重时可出现关节畸形。由于银屑病的发病机制复杂,目前医学手段尚未探清根本原理,但一般认为其主要原因是患者自体免疫机制发生紊乱,主要治疗手段以维生素、抗生素、靶向免疫制剂的生物药或化药为主。
在应对该疾病的治疗方面,生物制剂一直具有独到之地。自20世纪起,科学家们一直在探索其发病机制,从最早的角质形成细胞异常、辅助性T细胞平衡紊乱、再到后来的肿瘤坏死因子-α(TNF-α)、IL-17、IL-23等研究热度未减。
目前全球范围内可用于治疗该疾病且已获批上市的生物制剂可分为白介素类、TNF-α及T细胞抑制类。如靶向TNF-α的阿达木单抗、赛妥珠单抗、戈利木单抗,靶向 IL-17A的司库奇尤单抗、依奇珠单抗以及尼塔奇单抗。其中尼塔奇单抗是一种靶向IL-17A的嵌合型IgG1纳米单抗,已于俄罗斯上市,这种药物不仅针对银屑病及衍生关节炎有治疗作用,也可以用于强直性脊柱炎的治疗。

针对性治疗银屑病生物制剂及靶点[1]
随着生物制剂的不断开发,目前针对银屑病治疗的生物制剂中已进入临床II期或III期实验且显示有效的药物研发中以靶向IL-17信号通路及IL-23的研究为主。
一种靶向IL-36R的人源化单抗imsidolimab在临床II期试验中显示,患者在进行第1/4/16周的治疗后,严重性指数分别下降29%,54%,98%,而皮损面积分别下降60%,94%,98%,药物耐受性良好,且不良反应报告中仅具轻中性不良事件。另一种靶向IL-17A的单抗vunakizumab在II期试验中同样表现出耐受性良好,且未发现口腔念珠菌病、恶性肿瘤、炎症性肠病或重大心脏不良事件以及预期之外不良安全事件的发生[1]。
种种研究表明,生物制剂对于银屑病的疗效显著。但仍有一部分药物在受试患者的治疗试验中并未达到目标疗效。如阿达木单抗在治疗银屑病关节炎的长期给药过程中易导致抗药物抗体(ADAs)的形成,而随着ADAs的逐步堆积最终导致该药物的疗效丧失[4]。相比之下,同样可用于治疗自体免疫关节炎的另一种药物Ozoralizumab由Ablynx公司开发,这是一种抗TNF-α的人源化纳米抗体,由两个抗人TNF-α纳米抗体和一个抗人血清白蛋白 (HSA) 纳米抗体组成,其在临床实验中具有良好的亲和力以及耐受性,且未发现明显的ADAs形成。
在银屑病治疗方面,sonelokimab是一种由三个序列优化单价部分组成的纳米抗体,用于阻断IL-17A/F及其异二聚体。在临床II期的对照实验中显示,其应答率分别为90.2%,76.5%,33.3%,而司库奇优单抗对照组为90.6%,64.2%,28.3%。通过52周的治疗试验中发现,sonelokimab的安全性与司库奇优单抗相似,但其疗效、速度更好,且司库奇优单抗可能具有更高更频繁的口腔真菌感染发生概率[5]。
因而,生物制剂亟需新的成药策略来延长治疗时间以及避免疗效丧失的情况发生。
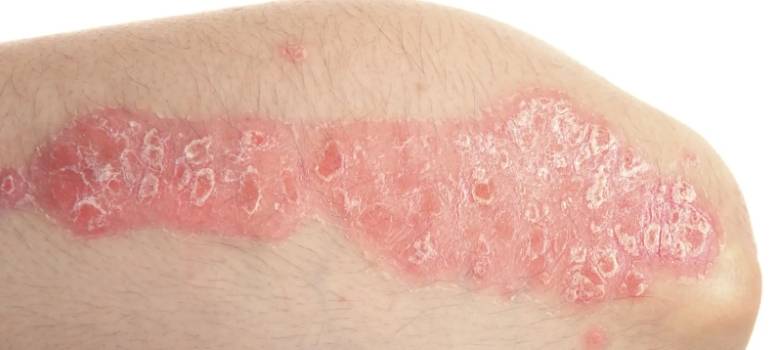
纳米抗体的各种优势在生物制剂领域广受青睐,其低免疫原性、易改造性以及极强的靶向能力使得纳米抗体在许多方面远优于传统抗体,也不失为一种新生物制剂的研发策略。
纳博生命专注于纳米抗体的开发、改造与应用,拥有符合实验动物标准的羊驼繁育基地与独立实验基地。致力于构建产、学、研一体化的实验公共服务平台。希望能为广大生物科研机构、医药研发企业和创新团队提供更专业、性价比更高的实验服务。欢迎各方研发人员与我们交流联系。