诸多研究表明EGFR在大多数实体肿瘤中均存在异常表达或过度表达,并已在肿瘤疾病中发现了EGFR的多种突变型,其突变型作用可能包括对细胞增殖的持续活化、信号通路的异常激活及抑制肿瘤细胞凋亡等。此外,研究发现EGFR可参与调节Ang-1及VEGF等因子的水平从而影响肿瘤微血管的形成[1]。此类机制的发现使得EGFR成为肿瘤治疗领域的热门靶点之一。
发表于Scientific Reports的《resence of EGF ligand restricts the binding ability of EgB4 nanobody to EGFR extracellular domain》研究通过分子动力学模拟等计算方法研究了EgB4纳米抗体对EGFR的特异性结合能力,这种纳米抗体可以无视其他阻力地与EGFR竞争性结合,且不会妨碍EGFR本身的功能,可促进癌症的抗体偶联药物的开发或药物递送[2]。
另一篇发表于PNAS的研究将抗EGFR纳米抗体与TRAIL(肿瘤坏死因子相关凋亡诱导配体)制备出ENb2-TRAIL,而后又将NSC(神经干细胞)与前者再次结合制备出NSC-ENb2-TRAIL。研究结果表明ENb2-TRAIL可以特异性地与EGFR相结合,并与EGF具有竞争性结合能力。可抑制EGFR的异常信号传导,对不同TRAIL敏感性的GBM(多形性胶质母细胞瘤)细胞系均有抑制作用;而后者具有的抑制能力则更强,在GBM小鼠模型中表现有显著的抑制肿瘤生长的特性,还可同时诱导GBM细胞凋亡,使肿瘤消退,明显延长小鼠生存期。该研究证实了抗EGFR特异性纳米抗体变体的治疗性干细胞具有显著抗肿瘤效果,为GBM的治疗提供了新的策略和理论依据[3]。
尽管此前单克隆抗体技术在靶向治疗药物的各种研究中获得广泛关注,但在某些目标分子的研究开发和验证中,传统抗体技术仍无法达成良好的效果,而利用新的抗体技术却能得到意想不到的结果。如EGFR的基因突变或间质-表皮转换因子(Met)旁路激活后,常使得机体对酪氨酸激酶抑制剂产生耐药性,为此我国中科大与浙江省肿瘤医院的联合研究团队以纳米抗体作为工具设计出一种可同时靶向突变型EGFR和Met的双特异性纳米抗体融合蛋白,以阻断他们在非小细胞癌中的相互作用。这种纳米抗体融合蛋白有效地抑制了EGFR和Met信号通路之间的相互作用,并进一步抑制了Erk及Akt等下游通路,同时诱导了包括Rb、p21及p27在内的细胞周期停滞相关蛋白的表达[4],这种靶向策略为肿瘤治疗的研究提供了一种新的思路。
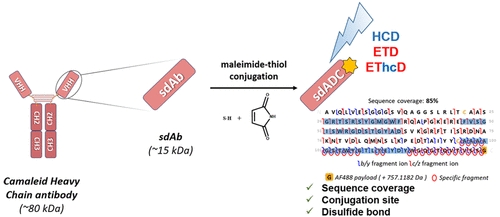
纳米抗体的高亲和力、易于改造及分子体积小的优势使得它在治疗性融合蛋白、抗体偶联药物等不同领域的研究中受到越来越多的关注。与传统抗体相比,这种由重链可变结构域形成的小型蛋白具有更强的靶向治疗能力和生产优势,它们可以进行不同的生物偶联过程以形成如纳米抗体药物偶联物(sdADCs)来提升治疗效力,并极大程度地降低了自身的免疫原性,同时还能保证自身优秀的靶向能力[5]。
纳米抗体药物偶联物及序列信息等
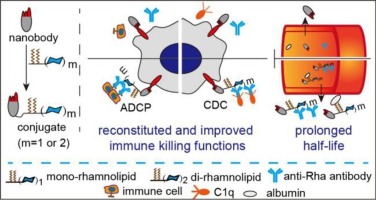
然而,纳米抗体的分子体积小的特点在一定程度上也成为了它的劣势,这种特点导致其半衰期明显短于传统抗体,使得纳米抗体在机体内会被迅速分解,但同时又因其具有优秀的改造能力可以使研究人员轻松的解决这种局限性。我国江南大学吴志猛团队设计合成了一种以鼠李糖(Rha)修饰的双特异性纳米抗体,这种纳米抗体是将靶向EGFR的纳米抗体7D12位点特异性地偶联到一系列鼠李糖脂衍生物上作为抗体招募分子,研究表明该分子可以将人体血清中存在的天然抗Rha抗体招募至肿瘤细胞表面,或与抗Rha抗体结合成为免疫复合物来达成激活Fc介导的免疫反应以及延长半衰期的双重目的[6]。该研究结果表明,将鼠李糖脂与纳米抗体特异性结合是一种足以提升纳米抗体对肿瘤免疫治疗功效的改造策略。
双特异性纳米抗体激活FC介导的免疫反应并延长半衰期示意图
纳米抗体凭借高亲和力、高穿透能力、精准靶向能力以及多功能改造潜力等独特优势为EGFR相关肿瘤治疗开辟了全新的路径,使其成为未来精准抗癌的重要工具。
纳博生命现拥有覆盖抗体开发到抗体发现,再到抗体工程的全链路技术平台。其中包括噬菌体展示、大肠杆菌展示、哺乳动物细胞展示等筛选平台,膜蛋白制备及mRNA免疫平台。通过多平台的交叉互补为药企及科研院所提供灵活的抗体发现及改造服务,助力药物试剂的研发。
纳博生命专注于纳米抗体开发、改造与应用,拥有符合实验动物标准的羊驼繁育基地与独立实验基地。致力于构建产、学、研一体化的实验公共服务平台。希望能为广大生物科研机构、医药研发企业和创新团队提供更专业、性价比更高的实验服务。
更多服务内容,请关注纳博生命公众号或拨打官方电话400-822-9180进行咨询!