GPCRs是药物研发领域中的热门,全球约30%的上市药物以其为作用对象。AT1R作为GPCR家族的代表性成员,通过结合AngII(内源性配体血管紧张素II)激活Gq蛋白信号通路,引发血管收缩等生理反应,其功能异常直接关联高血压、心肌肥厚等多种心血管疾病。尽管ARBs类降压药物已广泛应用,但传统拮抗剂存在作用机制单一、部分患者响应不佳等问题。
更关键的是,GPCR激活具有“偏向性信号传导”特性,即不同配体可选择性激活特定信号通路。如:已有研究表明β-arrestin偏向性AT1R激动剂能在不影响血压的前提下改善心肌收缩功能,为心力衰竭治疗提供了新方向。但肽类配体结合型GPCR构象具有高度动态、难以结晶的特点,且科研人员一直缺乏其活性状态的高分辨率结构,无法明确配体与受体的相互作用细节,也难以解释偏向性激动剂的作用机制。此前报道的AT1R晶体结构均为拮抗剂结合的失活态,与肽类激动剂的结合模式存在本质差异,亟需获取其活性态结构以填补研究空白。
本研究首次成功解析了人源AT1R在活性状态下的晶体结构,分辨率达2.9Å。该结构揭示了AT1R与部分激动剂S1I8肽的详细结合模式,并展示了一种由合成纳米抗体(Nb.AT110i1)稳定的受体构象。研究不仅阐明了AT1R的独特激活机制,还揭示了其与已知GPCR激活模式的显著差异,为理解偏向性信号传导提供了结构基础。
合成纳米抗体的筛选与优化
GPCR构象的动态性和不稳定性是结晶研究的主要障碍,而纳米抗体凭借其小尺寸、长抗原结合环等优势,成为稳定目标构象的理想工具。但传统免疫接种方法难以获得 AT1R 特异性纳米抗体,团队转而采用合成酵母展示纳米抗体库进行筛选。
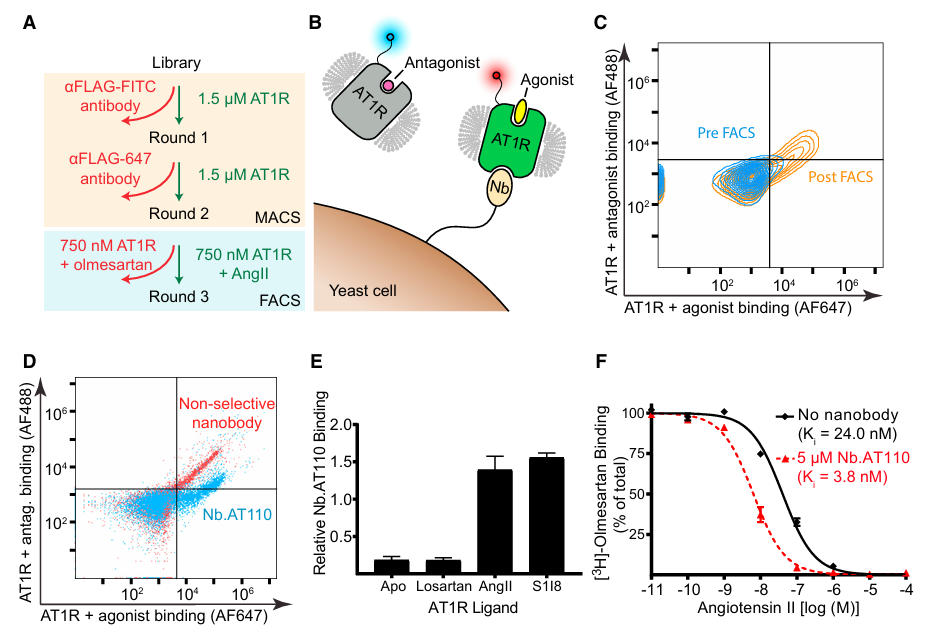
筛选过程分为两步:首先通过两轮MACS富集AT1R结合型纳米抗体,随后利用FACS筛选构象特异性克隆,将酵母与奥美沙坦结合的AT1R(AF488标记)和AngII激动剂结合的AT1R(AF647标记)共孵育,选择性收集与活性态AT1R结合的酵母克隆。最终获得高特异性纳米抗体Nb.AT110。研究发现,它仅在激动剂存在时与AT1R发生共免疫沉淀,并能将AngII对AT1R的亲和力提升约6倍。
图1:酵母展示技术筛选活性态 AT1R 特异性纳米抗体
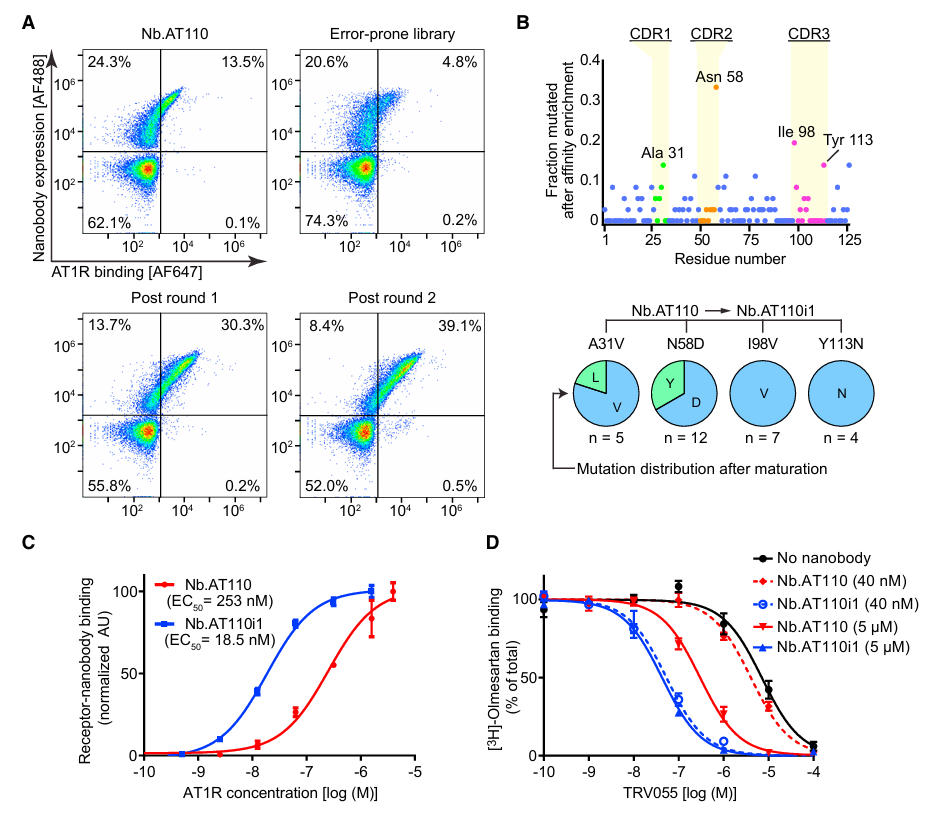
为满足结晶需求,团队通过易错PCR构建突变库,经两轮FACS亲和力成熟,筛选出含A31V、N58D、I98V、Y113N四个关键突变的变体Nb.AT110i1(图 2)。该变体对活性态 AT1R 的亲和力较原始抗体提升超 100 倍,为后续复合物结晶奠定了基础。
图2:Nb.AT110 的亲和力成熟
AT1R-配体-纳米抗体复合物结晶与结构解析
为解决传统AT1R结晶构建体亲和力低下的问题,团队重新设计了蛋白质表达与结晶的构建体。在第三细胞内环(ICL3)插入热稳定蛋白BRIL,保留N端完整序列,以避免影响肽类配体结合,并进行C端截短。该构建体对AngII的亲和力较野生型提升2倍,且能与Nb.AT110i1稳定结合。
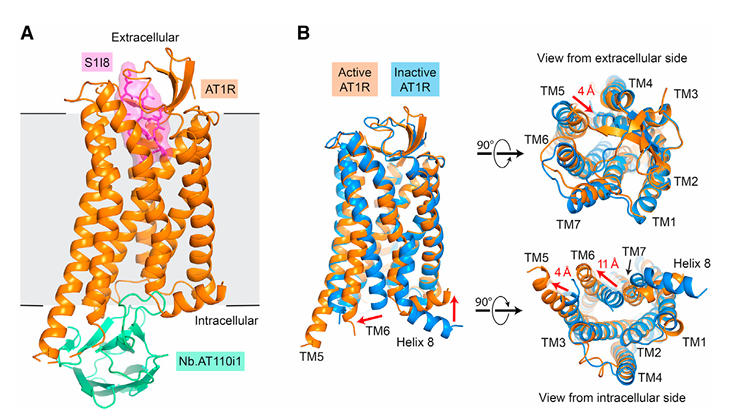
研究选用AngII类似物S1I8作为配体,与AT1R、Nb.AT110i1形成三元复合物,通过脂立方相结晶法获得衍射质量晶体。整合5个晶体的衍射数据后,利用分子置换法解析出2.9Å分辨率的晶体结构。结构显示,Nb.AT110i1结合于AT1R的细胞内转导子口袋,其超长CDR3环插入受体核心区域,稳定了活性态特有的构象变化。
图3:Nb.AT110i1稳定的AT1R活性态结构
AT1R激活机制与配体结合模式的揭示
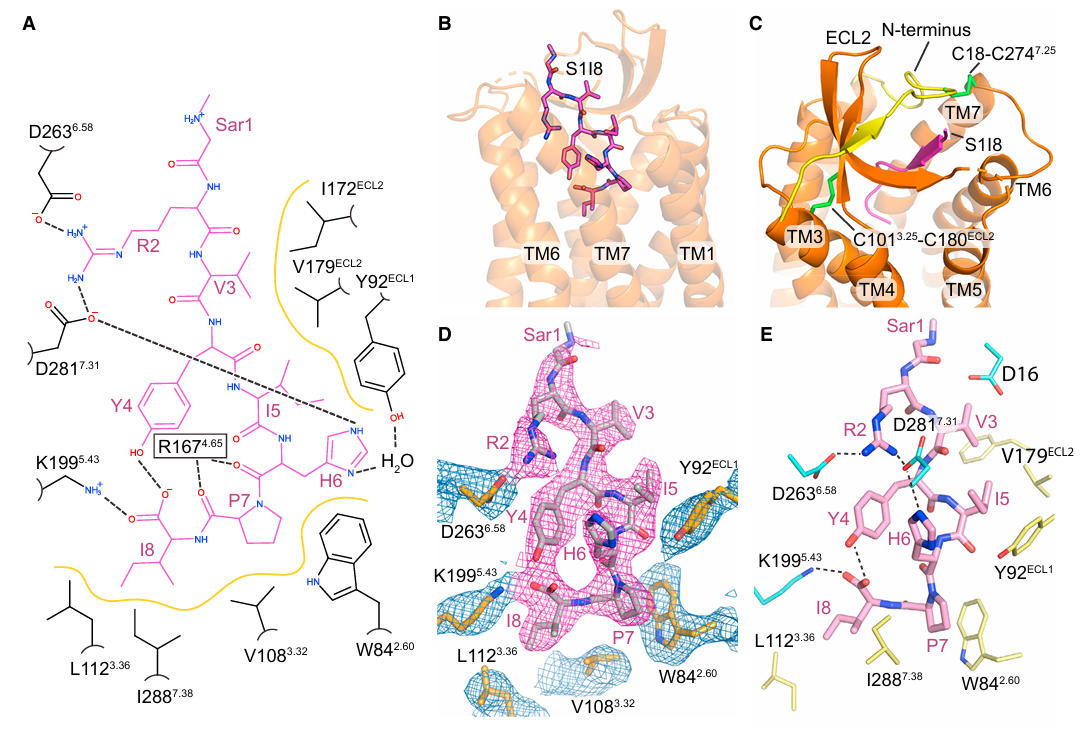
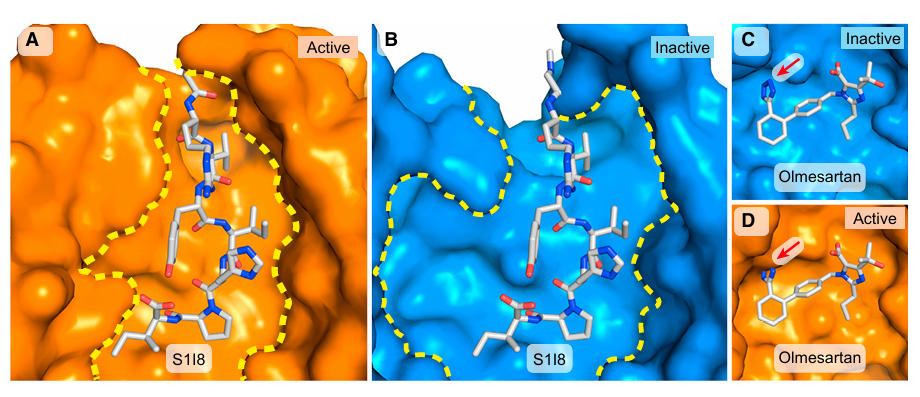
结构分析发现,AT1R的激活机制具有独特性:S1I8以延伸构象结合于受体口袋,N端朝向细胞外溶剂,C端深埋于受体核心,通过极性与疏水作用形成广泛界面。
图4:S1I8与AT1R的结合模式
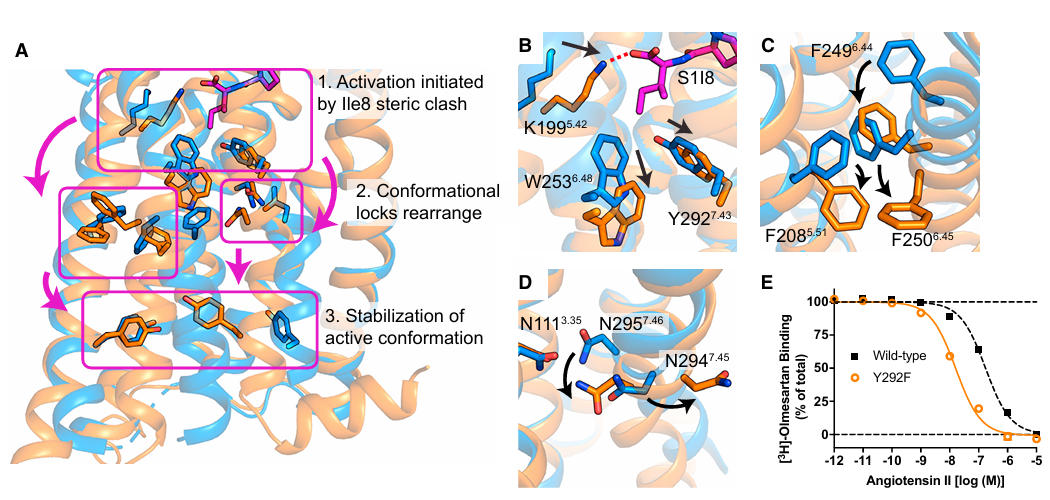
配体C端的I8残基与受体K1995.42等位点的相互作用引发构象级联反应——W2536.48与Y2927.43向下位移,触发TM5与TM6 间的苯丙氨酸棘轮重排,最终导致TM6向外位移11Å,形成G蛋白结合位点。
图5: AT1R的激活机制
与其他GPCR不同,AT1R通过N1113.35与 N2957.46的氢键替代钠离子稳定失活态,且其活性态结合口袋经TM5、TM7向内位移显著收缩,与拮抗剂结合的失活态口袋形成明显差异,解释了ARBs类药物反向激动作用的特性,这种特性不仅阻断激动剂作用,还能抑制受体的基础活性。此外,S1I8与AT1R的N端、ECL2形成独特的半β桶结构,即肽链与受体片段共同形成了一个不完整的β桶状结构,这种结合模式在肽类GPCR中较为独特。这一结合模式为肽类GPCR的配体识别机制提供了新认知。
图6:活性态与失活态AT1R结合口袋的差异
偏向性信号传导的结构基础验证
团队通过DEER光谱分析证实,AT1R的构象集合(conformational ensemble)与配体类型密切相关:AngII全向激动剂稳定的构象与晶体结构高度一致,而β-arrestin偏向性激动剂则稳定不完全激活的构象。结构显示,配体C端残基的体积差异是偏向性的关键,F8的苯环结构引发受体核心更大程度的构象重排,而小体积残基则无法完全触发这一过程,导致信号传导偏向β-arrestin通路。这一发现为设计高选择性偏向性药物提供了明确的结构靶点。
本研究不仅首次揭示了AT1R的活性结构,更展示了合成纳米抗体在GPCR结构生物学中的强大潜力。Nb.AT110及其变体仅在激动剂存在时与AT1R结合,不与失活态受体或其他GPCR交叉反应,这种精准靶向性确保了活性态构象的稳定捕获,解决了 GPCR 结构研究中构象异质性的核心难题。随着这类工具与方法的推广,未来我们将有望看到更多“难以捉摸”的膜蛋白结构被解析,为药物研发与疾病治疗带来革命性突破。

武汉纳博生命科技有限公司是由武汉产业创新发展研究院牵头成立建设的纳米抗体产业平台。其总部位于武汉东湖新技术开发区武创院本部大楼,在武汉生物城精准医疗产业基地拥有占地面积达1400㎡的自主实验室,并在武汉左岭与黄冈团风分别建立了符合实验动物标准的羊驼实验基地与转运基地,目前基地在饲养的羊驼共600余头,可为科研机构及抗体药物研发企业提供“零免疫背景”保障的羊驼免疫服务。
纳博生命专注于纳米抗体开发、改造与应用,致力于构建产、学、研一体化的实验公共服务平台。现拥有从抗原制备(多肽、蛋白及RNA),到抗体发现和抗体工程,再到生物学功能验证/筛选的全链路技术平台。其中RNA抗原包括针对羊驼进行RNA结构和序列优化的RNA;抗体发现与抗体工程服务采用噬菌体展示、RNA以及哺乳动物细胞展示在内的多种技术路线。通过多平台的交叉互补为药企及科研院所提供灵活的抗体发现及改造服务,助力药物试剂的研发。
联系方式:400-822-9180 丨 联系邮箱:marketingdept@nanobodylife.com